Western Equine Encephalomyelitis (WEE) is een ziekte die sporadisch optreedt bij paarden en mensen, en die wordt overgebracht door muggen. Vogels zijn tussengastheer, maar het virus kan ook circuleren in populaties van prairiehazen. Paarden en mensen zijn eindgastheer van dit virus. De ziekte wordt gekenmerkt door koorts, anorexie en soms ernstige depressie en diverse andere neurologische verschijnselen. WEE is veel minder vaak fataal (case fatality rate 20-40 procent) dan Eastern Equine Encephalomyelitis (EEE) bij paarden (case fatality rate 50-90 procent) indien er neurologische verschijnselen optreden. Ook sommige vogelsoorten, met name emoes, kunnen ziekteverschijnselen vertonen.
Direct naar:
De kiem
WEE wordt veroorzaakt door een virus van het geslacht Alphavirus van de familie van de Togavirussen. Western Equine Encephalomyelitis Virus (WEEV) is nauw verwant aan andere alphavirussen zoals Sindbis en Highlands J-virussen. Phylogenetische studies laten zien dat WEEV-isolaten recombinanten zijn van EEEV-like virussen (2/3 van het genoom) en Sindbis-like virussen (1/3 van het genoom). De virussen circuleren onder vogels en muggen van midzomer tot laat in de herfst. WEEV kan worden geïsoleerd uit de hersenen van gestorven paarden, met name als er minder dan 5 dagen zijn verlopen tussen de eerste verschijnselen en de sterfte. Virusisolatie uit bloed en cerebrospinale vloeistof lukt zelden.
Gevoelige diersoorten
Meer dan 25 verschillende muggensoorten zijn mogelijke vectoren van WEEV. De belangrijkste is Culex tarsalis (transmissie van vogel naar vogel). Aedes spp en Ochlerotatus melanimon zijn de belangrijkste brugvectoren (transmissie vogel naar mens/paard). Vogels zijn de natuurlijke gastheren van het virus. Na overspill vanuit het vogelreservoir kan het virus ook in prairiehazen circuleren. Het overwinteringsmechanisme van dit virus is eigenlijk onbekend; zowel verticale transmissie in muggen als persistentie in reptielen wordt gesuggereerd. Infecties bij slangen, kikkers en schildpadden zijn beschreven.
Paarden kunnen worden besmet, maar zijn eindgastheer en zijn niet infectieus voor andere paarden. Datzelfde geldt voor mensen. Daarnaast zijn asymptomatische infecties beschreven bij eekhoorns, slangen, kikkers en schildpadden en sommige in het wild levende zoogdieren. Bij emoes kan WEEV milde tot ernstige ziekteverschijnselen veroorzaken, waarbij anorexie, lusteloosheid, gewichtsverlies, diarree en neurologische verschijnselen gerapporteerd zijn. Bij kalkoenen kan WEEV een daling in de eiproductie veroorzaken met een toename aan schaalloze en kleine, bleke eieren.
Volksgezondheid
Mensen zijn, evenals paarden, gevoelig voor infectie met WEEV. De incubatieperiode van WEE is meestal 5 tot 10 dagen. In Noord-Amerika treden gemiddeld 34 bevestigde WEE- gevallen per jaar op, met name bij kinderen jonger dan 15 jaar en volwassenen ouder dan 55 jaar. De ratio tussen encephalitis en asymptomatische infecties of aspecifieke ziekteverschijnselen is globaal 1:1 in kinderen onder een jaar, 1:55 in kinderen van 1 tot 4 jaar en 1:1000 in volwassenen. De mortaliteit van WEE (dus de case fatality ratio bij optreden van neurologische verschijnselen) is 3 tot 7 procent (dit in tegenstelling tot EEE waarbij de mortaliteit de 70% benadert), dit kan bij jonge kinderen overigens veel hoger zijn. Mensen met neurologische verschijnselen die de infectie overleven blijven echter vaak permanent last houden van de nasleep van de ziekte. Ongeveer 5 tot 30 procent van de jonge patiënten heeft permanente neurologische schade. Ernstige infecties en sterfte zijn gevonden bij laboratoriummedewerkers. Daarom dient werk aan deze virussen uitsluitend in laboratoria met isolatieniveau 3 te geschieden. Sinds 1964 zijn er minder dan 700 bevestigde gevallen opgetreden in de USA. In de laatste jaren is de incidentie van humane WEEV infecties drastisch afgenomen, het laatste gedocumenteerde humane geval dateert van 1994 en de laatste positieve muggenpool werd in 2008 gevonden.
Overleving
WEEV overleeft niet buiten de gastheer, dus persisteert niet in de omgeving.
Desinfectie
WEEV is gevoelig voor de meeste gebruikelijke desinfectantia (NatriumHypochloriet, Halamid, formaline, ethanol, glutaaraldehyde). Het virus is gevoelig voor vochtige en droge verhitting en voor droogte.
Terug naar het begin van dit artikel
Klinisch beeld
Na een incubatietijd van 5 tot 14 dagen beginnen de klinische verschijnselen van een WEE-infectie bij paarden meestal met koorts, gebrek aan eetlust en depressie. In de ernstige gevallen volgt een ontsteking van hersenen, ruggenmerg en hersenvliezen. Humaan zijn WEE-infecties gekenmerkt door acuut optredende hoofdpijn met koorts en aseptische meningitis. In ernstige gevallen is er sprake van hoge koorts, hevige hoofdpijn, trillingen, spasmen, krampen en verlammingen. De meest ernstige ziekteverschijnselen worden gezien bij kinderen onder een jaar en met name onder drie maanden leeftijd. De laatste groep blijft last houden van epileptische aanvallen als er zich in het acute stadium convulsies voordeden.
Bij paarden zijn de meest kenmerkende neurologische verschijnselen excitatie, blindheid, ataxie, ernstige mentale depressie, verlamming, krampen en sterfte. WEE staat in de differentieeldiagnose bij niet gevaccineerde paarden die de karakteristieke slaperigheid vertonen gedurende de zomer in gematigde klimaatzones of gedurende het regenseizoen in tropische en subtropische regio’s. Echter: andere door muggen overgebrachte ziekten zoals West Nile Fever geven dezelfde klinische verschijnselen. In het laatste decennium worden er slechts sporadisch klinische WEE-infecties bij paarden gerapporteerd, waarschijnlijk ten gevolgde van toegenomen vaccinatiegraad en optreden van subklinische infecties, waarbij ook immuniteit geïnduceerd wordt.
Morbiditeit/mortaliteit
In 1937-1938 werden meer dan 350.000 paarden en muildieren in de USA en Canada ziek ten gevolge van WEE-infecties. Sinds veel paarden gevaccineerd worden tegen WEE is de morbiditeit en mortaliteit aanzienlijk gedaald en komt het meestal als individuele gevallen voor. Bij paarden met neurologische verschijnselen is de case fatality ratio bij WEE meestal 20-30 procent. Bij met WEEV geïnfecteerde emoes varieerde de morbiditeit tussen 15 en 50 procent en de mortaliteit was ongeveer 9 procent.
Uitscheiding van de kiem
Bij paarden en mensen is er geen sprake van uitscheiding van de kiemen. Besmetting vindt plaats door muggen die bij vogels hun bloedmaal hebben opgenomen. De viremie in vogels duurt 2 tot 5 dagen. Muggen blijven echter levenslang reservoir, en verticale transmissie naar muggeneieren is mogelijk. Het virus overwintert waarschijnlijk in (eieren van) muggen en in vogels, knaagdieren, vleermuizen, reptielen en amfibieën
Differentieel diagnostiek
Zonder diagnostische testen is geen onderscheid te maken met West Nile Virus. Omdat geen enkel verschijnsel specifiek is, komen veel ziekten in aanmerking, zoals Venezuelan Equine Encephalomyelitis (VEE) en EEE, West Nile Fever, Afrikaanse Paardenpest, Rabiës, Infectieuze Anemie, Equine Herpesvirus Myeloencephalopathie (EHM), in Amerika Equine Protozoal Myeloencephalitis (EPM), vermineuze encephalopathie, neuroborreliose, cervicale vertebrale stenose, diverse vergiftigingen, Botulisme, Leverkolder en trauma.
Terug naar het begin van dit artikel
Pathologie
Grove pathologische laesies ontbreken vaak bij paarden. Hoogstens zijn congesties van de hersenen en meningen te zien. Eventueel worden puntbloedingen door trauma waargenomen. Microscopische laesies worden gewoonlijk wel aangetroffen in het gehele zenuwstelsel en zijn van diagnostische waarde. Er is een wijdverspreide ontstekingsreactie in de grijze hersensubstantie. Degeneratie en necrose van neuronen met gliosis en infiltratie van ontstekingscellen treedt vaak op. Perivasculaire ophopingen van lymfocyten en neutrofielen zijn te zien. De mate van voorkomen van laesies hangt af van de ernst van de infectie en de duur van de neurologische verschijnselen. WEEV kan via immunohistochemie, maar ook via in situ hybridisatie of RT-PCR, rechtstreeks op hersenmateriaal worden aangetoond
Isolatie van de kiem
Het WEE-virus kan worden geïsoleerd uit de hersenen van gestorven paarden en uit weefsels zoals lever of milt. Het is echter wel moeilijk om WEEV te isoleren. Op zich zijn diverse kweeksystemen geschikt (Vero, BHK-21, RK-13, geëmbryoneerde kippeneieren). Materiaal moet binnen 48 uur na gekoelde bewaring worden onderzocht. Indien dit niet mogelijk is dient het te worden ingevroren en onder droog ijs te worden verzonden. Vriezen verkleint echter de kans op virusisolatie aanzienlijk. Er bestaat een groot gevaar op humane infectie bij de virusisolatie uit besmette vogels door aërosolvorming van uiterst infectieus virus. WEEV kan met behulp van RT-PCR worden aangetoond in muggen en in weefsels van vogels en paarden. In landen zonder de faciliteiten voor virusisolatie of PCR kan ook een ELISA worden gebruikt voor het vaststellen van de besmettingsgraad in muggen.
Serologie
Voor het aantonen van antistoffen zijn de CBR, de haemagglutinatie-reductietest (HI-test), een IgM capture ELISA en een Plaque Reductie Neutralisatie Test (PRN-test) beschikbaar. De IgM capture ELISA kan naast serum ook op CSF gebruikt worden, maar dit geeft bij paarden minder consistente resultaten dan in serum (dit in tegenstelling tot de humane diagnostiek). WEE-infecties kunnen worden aangetoond in gepaarde sera, genomen met 10 tot 14 dagen tussentijd. Een viervoudige titerstijging is vereist voor het bevestigen van de diagnose. Meestal hebben paarden met klinische verschijnselen zeer hoge titers tegen WEEV. Detectie van IgM met een capture enzyme ELISA geeft een snelle voorlopige diagnose bij een acute infectie. De PRN-test, of de combinatie van de PRN-test met de HI-test, is het betrouwbaarst voor het aantonen van antistoffen. De CBR toont antistoffen tegen WEEV later aan en de reactie blijft niet positief. Daardoor is de CBR minder bruikbaar voor de serologische diagnostiek. In de CBR- en de HI-testen kunnen kruisreacties optreden met antilichamen tegen WEEV en EEEV. De PRN-test is het meest specifiek en kan gebruikt worden om onderscheid te maken tussen antistoffen gericht tegen EEEV dan wel WEEV.
Terug naar het begin van dit artikel
Nederland
WEE komt in Nederland niet voor.
Andere landen
Europa
EEE en WEE komen niet voor in Europa.
Landen buiten Europa
WEE komt voor van Argentinië tot West Canada. In de USA wordt het virus geïsoleerd westelijk van de Mississippi. Voor gedetailleerde informatie over de verspreiding zie: OIE: World Animal Health Situation en OIE bulletin (
www.oie.int)
Terug naar het begin van dit artikel
Vaccinatie
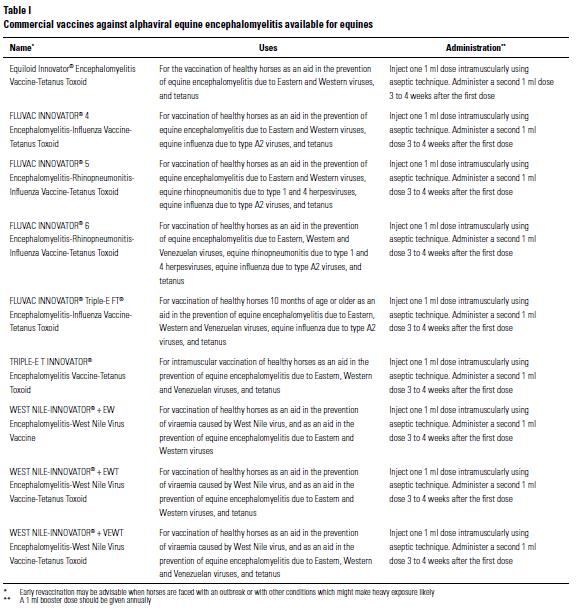
Er zijn in de USA diverse goede vaccins voor paarden beschikbaar. Met een goed vaccinatieschema is WEE bij paarden volledig te voorkomen. Fokmerries moeten een maand voor het veulenen worden gevaccineerd om een goede overdracht van maternale antistoffen via de biest te realiseren. Veulens uit goed gevaccineerde merries moeten vervolgens op een leeftijd van 6, 7, en 9 maanden gevaccineerd worden. Indien de merrie niet is gevaccineerd dient dit al te gebeuren op 4, 5 en 7 maanden. Vervolgens moeten in endemische gebieden paarden na de veulen vaccinaties drie keer per jaar gevaccineerd worden, dus met intervallen van 4 maanden. Vanaf een leeftijd van vier jaar kan vervolgens volstaan worden met twee keer per jaar vaccineren. De meeste vaccins zijn geïnactiveerde volvirusvaccins die tijdig moeten worden toegediend (starten met een basisimmunisatie van drie vaccinaties). Vaak betreft het combinatievaccins voor EEE, WEE en VEE. Bij niet gevaccineerde paarden dient altijd gestart te worden met het basis immunisatie schema. Er zijn geen humane vaccins geregistreerd. Wel worden er in de USA bepaalde groepen militairen en laboratoriumpersoneel gevaccineerd. Deze vaccins geven een acceptabele antistof respons gecorreleerd met bescherming. Zie verder onderstaande tabel voor commerciële vaccins voor de diverse veroorzakers van equine encephalomyelitis bij paarden.
Antibiotica/therapie
Er is geen specifieke behandeling. De behandeling van neurologische patiënten bestaat uit ondersteunende therapie met goede verzorging, NSAIDs, zo nodig infusen en electrolyten en anti-epileptica. Er zijn geen specifieke virostatica met een bewezen werking tegen WEE-infecties bij het paard. Burke et al. toonden in een muizenmodel aan dat zowel neutraliserende als niet-neutraliserende monoclonale antistoffen na intraveneuze toediening beschermden tegen een WEEV aerosol challenge.
Overige maatregelen
Bescherming van paarden
Besmette paarden zijn niet direct infectieus voor de omgeving. Paardenvliegendekens geïmpregneerd met permetrin kunnen de infectieoverdracht door muggen beperken. Ventilatoren in de stallen verlagen de muggendruk, evenals het bespuiten van de stalmuren met insecticiden. Opstallen kan het beste plaatsvinden voordat de schemering invalt en gedurende de nacht. De muggenactiviteit is het hoogst tussen zonsondergang en zonsopgang.
Algemene maatregelen
De hoogste veiligheidseisen met betrekking tot laboratoriummedewerkers zijn geboden (niveau 3 biosecurity). Naast vaccinaties van eerder genoemde categorieën personen zijn quarantainemaatregelen nodig, samen met een onderzoek naar de verspreiding. Voor dit laatste is onderzoek nodig van zowel de muggen als het bloed van de paarden in de omgeving.
Maatregelen in kader volksgezondheid
Communicatie en publieksvoorlichting zijn van groot belang. Deze communicatie dient zich te richten op algemene maatregelen ter voorkoming van vector-overdraagbare (in dit geval door muggen overdraagbare) ziekten. Deze adviezen zullen met name betrekking moeten hebben op het reduceren van muggenpopulaties door het weghalen van alle bronnen met stilstaand water in en om het huis, het dragen van bedekkende kleding, het gebruik van repellents zoals DEET en eventueel het gebruik van muskietennetten/klamboes en insecticiden in de directe omgeving (voor zover toegestaan binnen de Nederlandse wetgeving).
Terug naar het begin van dit artikel
Bedrijfshygiëne /insleeppreventie
Muggenbestrijding is in de praktijk moeilijk uitvoerbaar. Een aantal praktisch uitvoerbare (preventieve) maatregelen in de directe omgeving van mens en dier is behandeld in hoofdstuk 5.
Vaccinatie
Voor paarden zijn vaccins beschikbaar. In hoeverre deze in Nederland zullen mogen worden toegepast is onduidelijk. Daarnaast wordt muggenbestrijding en het gebruik van muggendekens, DEET, enzovoorts, aanbevolen.
Terug naar het begin van dit artikel
Nederlands recht
WEE is in Nederland volgens de Europese Diergezondheids Verordening (AHR) een aangifteplichtige ziekte.
Europees recht
WEE is een meldingsplichtige ziekte volgens de Europese diergezondheidsverordening (Animal Health Regulation AHR). Sinds 21 april 2021 valt het voorkomen en bestrijden van dierziekten onder deze Europese verordening. WEE valt net als EEE in categorie E.
De dierziekten in de Europese Diergezondheidsverordening zijn ingedeeld in de vijf categorieën A, B, C, D en E. Voor alle ziekten uit deze categorieën geldt een meldingsplicht, voor de ziekten uit categorieën A en B geldt daarnaast ook een bestrijdingsplicht.
• Dierziekten van categorie A zijn ziekten die niet in de Europese Unie voorkomen en die lidstaten meteen moeten uitroeien. Bijvoorbeeld mond-en-klauwzeer en varkenspest. Lidstaten moeten deze ziekten snel opsporen, direct bestrijden en besmette bedrijven en de directe omgeving afsluiten.
• Dierziekten van categorie B zijn ziekten die de Europese Unie wil uitroeien. Bijvoorbeeld tuberculose bij koeien, stieren en buffels. Lidstaten moeten deze ziekten daarom verplicht bestrijden. Lidstaten waar de ziekte niet voorkomt moeten maatregelen nemen om vrij te blijven van de ziekte.
• Dierziekten van categorie C zijn ziekten die minder besmettelijk zijn en die de Europese Unie wil indammen. Bijvoorbeeld de ziekte van Aujesky bij varkens en koeiengriep bij runderen. Lidstaten bepalen zelf of ze de ziekte willen uitroeien en of ze bij een uitbraak bedrijven afsluiten om verdere verspreiding te voorkomen.
• Dierziekten van categorie D zijn dierziekten die zich via internationale handelaren, vervoerders of reizigers verspreiden en die de Europese Unie wil indammen. Bijvoorbeeld abortus blauw bij varkens en verkoudheid (mycoplasma) bij kippen. Landen moeten voldoen aan Europese regels voor vervoer van en naar de EU en erbinnen.
• Dierziekten van categorie E zijn dierziekten die in de gaten gehouden moeten worden. Bijvoorbeeld Q-koorts bij geiten en paratuberculose bij runderen. Lidstaten moeten zich houden aan Europese regels om deze ziekten te melden.
WEEV komt voor op de lijst van ‘goederen’ die zijn opgenomen in bijlage I bij Besluit 1999/193/GBVB van de Raad van 9 maart 1999 tot wijziging van Besluit 94/942/GBVB betreffende het Gemeenschappelijk optreden. Dit is door de Raad vastgesteld op grond van artikel J.3 van het Verdrag betreffende de Europese Unie, ten aanzien van de controle op de uitvoer van goederen voor tweeërlei gebruik.
Internationaal
Het verkeer van paarden binnen de EU en de invoer van paarden vanuit derde landen is geregeld in Richtlijn 90/426/EEG van de Raad van 26 juni 1990 tot vaststelling van veterinairrechtelijke voorschriften voor het verkeer van paardachtigen en de invoer van paardachtigen uit derde landen. Hierin staan alleen specifieke bepalingen voor Afrikaanse paardenpest, VEE, Dourine en kwade droes genoemd, zoals hieronder aangegeven. Wel kunnen volgens artikel 13 lid 2b aanvullende waarborgen geëist worden voor ziekten die in de Gemeenschap exotisch zijn.
Artikel 13
1. De paardachtigen moeten afkomstig zijn uit derde landen:
a) die vrij zijn van paardenpest;
b) die sedert twee jaar vrij zijn van Venezolaanse paardenencefalomyelitis (VEE);
c) die sedert zes maanden vrij zijn van dourine en van kwade droes.
2. Volgens de procedure van artikel 24 kan de Commissie
a) beslissen dat lid 1 slechts voor een gedeelte van het grondgebied van een derde land geldt. In geval van regionalisering van de vereisten ten aanzien van paardenpest dienen ten minste de in artikel 5, leden 2 en 3, genoemde maatregelen in acht te worden genomen;
b) aanvullende waarborgen eisen voor ziekten die in de Gemeenschap exotisch zijn.
Terug naar het begin van dit artikel
Websites
Literatuur
- Acha PN, Szyfres B [Pan American Health Organization (PAHO)]. Zoonoses and communicable diseases common to man and animals. Volume 2. Chlamydioses, rickettsioses, and viroses. 3rd ed. Washington DC: PAHO; 2003. Scientific and Technical Publication No. 580. Western equine encephalitis; p. 365-372.
- Ayers JR, Lester TL, Angulo AB. An epizootic attributable to western equine encephalitis virus infection in emus in Texas. J Am Vet Med Assoc. 1994;205:600-1.
- Aréchiga-Ceballos N, Aguilar-Setién A. Alphaviral equine encephalomyelitis (Easter, Western and Venezuelan). Rev Sci Tech Off Int Epiz 2015; 34 (2): 491-501
- Burke CW, Froude JW, Miethe S, Hülseweh B, Hust M, Glass PJ. Human-Like Neutralizing Antibodies Protect Mice from Aerosol Exposure with Western Equine Encephalitis Virus. Viruses. 2018 Mar 24;10(4).
- Calisher CH. Medically important arboviruses of the United States and Canada. Clin Microbiol Rev. 1994;7:89-116.Centers for Disease Control and Prevention (CDC). Information on arboviral encephalitides [online]. CDC; 2005 Nov. Available at: http://www.cdc.gov/ncidod/dvbid/arbor/arbdet.htm.
- Chin J, editor. Control of communicable diseases. Washington, D.C.: American Public Health Association; 2000. Arthropod–borne viral diseases; p. 28-47.
- Cooper GL, Medina HA. Egg production drops in breeder turkeys associated with western equine encephalitis virus infection. Avian Dis. 1999;43:136-41.
- Dupuy LC, Richards MJ, Livingston BD, Hannaman D, Schmaljohn CS. A Multiagent Alphavirus DNA Vaccine Delivered by Intramuscular Electroporation Elicits Robust and Durable Virus-Specific Immune Responses in Mice and Rabbits and Completely Protects Mice against Lethal Venezuelan, Western, and Eastern Equine Encephalitis Virus Aerosol Challenges. J Immunol Res. 2018 Jun 3;2018.
- Fulhorst CF, Hardy JL, Eldridge BF, Presser SB, Reeves WC. Natural vertical transmission of western equine encephalomyelitis virus in mosquitoes. Science. 1994;263:676-8.
- Hu WG, Steigerwald R, Kalla M, Volkmann A, Noll D, Nagata LP. Protective efficacy of monovalent and trivalent recombinant MVA-based vaccines against three encephalitic alphaviruses. Vaccine. 2018 Aug 16;36(34):5194-5203.
- Leake CJ. Mosquito–borne arboviruses. In: Palmer SR, Soulsby EJL, Simpson DIH, editors. Zoonoses: Biology, clinical practice and public health control. New York: Oxford University Press; 1998. p.401–413.
- Long MT. West Nile Virus and Equine Encephalitis Viruses – New Perspectives. Vet Clin Equine 2014; 30: 523-542.
- Nandalur M, Urban AW. Western equine encephalitis [online]. eMedicine; 2007 Oct. Available at: http://www.emedicine.com/MED/topic3156.htm.
- Public Health Agency of Canada, Office of Laboratory Security. Material Safety Data Sheet: Western equine encephalitis virus, Eastern equine encephalitis virus [online]. Office of Laboratory Security; rel="noopener noreferrer" 2001 Jan. Available rel="noopener noreferrer" at:http://www.phac-aspc.gc.ca/msds-ftss/msds52e.html.
- Reisen WK, Chiles RE, Martinez VM, Fang Y, Green EN. Experimental infection of California birds with western equine encephalomyelitis and St. Louis encephalitis viruses. J Med Entomol. 2003;40:968-82.
- Schmaljohn AL, McClain D. Alphaviruses (Togaviridae) and flaviviruses (Flaviviridae). In: Baron rel="noopener noreferrer" S, editor. Medical microbiology rel="noopener noreferrer" [online]. 4th ed. New York: Churchill Livingstone; 1996. Available at: http://www.gsbs.utmb.edu/microbook/ch054.htm.
- World Organization for Animal Health [OIE] . Manual of diagnostic tests and vaccines for terrestrial rel="noopener noreferrer" animals [online]. Paris: OIE; 2008. Equine encephalomyelitis (eastern and western). Available at: http://www.oie.int/eng/normes/mmanual/A_00081.1. Acha PN, Szyfres B [Pan American Health Organization (PAHO)]. Zoonoses and communicable diseases common to man and animals. Volume 2. Chlamydioses, rickettsioses, and viroses. 3rd ed. Washington DC: PAHO; 2003. Scientific and Technical Publication No. 580. Western equine encephalitis; p. 365-372.
Terug naar het begin van dit artikel