Eastern Equine Encephalomyelitis (EEE) is een ziekte die sporadisch optreedt bij paarden en mensen, en die wordt overgebracht door muggen. Vogels zijn tussengastheer van dit virus, paarden en mensen zijn eindgastheer. De ziekte wordt gekenmerkt door koorts, anorexie, ernstige depressie en diverse andere neurologische verschijnselen. EEE is meestal fataal bij paarden en mensen indien er neurologische verschijnselen optreden (case-fatality rate > 90 procent).
Direct naar:
EEE wordt veroorzaakt door een virus van het geslacht Alphavirus van de familie van de Togavirussen. De Eastern Equine Encephalomyelitis Virus-isolaten (EEEV-isolaten) kunnen in twee varianten (voorheen vier lijnen) gegroepeerd worden. De variant die in de USA gevonden wordt (lineage I), was meer pathogeen dan de varianten die voorkomen in Zuid- en Centraal-Amerika (lineage II, III en IV). Deze laatste drie lineages zijn nu een nieuwe virus species geworden, het Madariaga virus. In 2008 en 2009 werden er echter grote uitbraken met hogere morbiditeit en mortaliteit gezien in Centraal en Zuid Amerika. In Brazilie vertoonden bijvoorbeeld 229 paarden ziekteverschijnselen ten gevolge van EEE infecties met een case-fatality rate van 73 procent en een vergelijkbare ernst van de ziekteverschijnselen t.o.v. Noord-Amerikaanse isolaten. De virussen circuleren tussen vogels en muggen van midzomer tot laat in de herfst. Recent zijn slangen ook als mogelijk reservoir beschreven. EEEV kan worden geïsoleerd uit de hersenen van eraan gestorven paarden, maar dat lukt alleen als er minder dan 5 dagen zijn verlopen tussen de eerste verschijnselen en de sterfte.
Er zijn meer dan 25 verschillende muggensoorten bekend als mogelijke vector van EEEV. De belangrijkste is Culiseta melanura (USA en Canada, zorgen voor transmissie van vogel naar vogel). Aedes spp, Coquillettidia perturbans en Culex spp. zijn de belangrijkste brugvectoren (transmissie vogel naar mens/paard). Vogels zijn de natuurlijke gastheren van het virus. Het overwinteringsmechanisme van dit virus is nog niet definitief opgehelderd: zowel verticale transmissie in muggen als persistentie in reptielen (met name slangen) wordt gesuggereerd. Daarnaast kan het virus worden overgedragen door luizen en mijten.
Paarden en mensen kunnen worden besmet, maar zijn eindgastheer en zijn in principe vervolgens niet infectieus voor andere paarden en/of mensen, al kunnen paarden soms een kortdurende viraemie ontwikkelen die hoog genoeg is om muggen te infecteren. Het virus is niet infectieus voor de meeste andere zoogdieren dan mens en paard, al is het virus ook geïsoleerd uit de hersenen van een hond met encephalitis en kan EEEV ziekte veroorzaken bij varkens. Bij kalkoenen veroorzaakt EEEV depressie, verlaagde eiproductie en verhoogde sterfte. Hoewel het virus meestal wordt overgebracht door muggen verspreidt het zich binnen een koppel gedomesticeerde vogels vooral door veren pikken en kannibalisme.
EEEV veroorzaakt een hoge mortaliteit bij in gevangenschap gehouden siervogels, zoals fazanten, patrijzen, kwartels en casuaris vogels. EEE veroorzaakt haemorrhagische enteritis met een hoge mortaliteit en morbiditeit bij struisvogels en emoes.
Volksgezondheid
Mensen zijn evenals paarden erg gevoelig voor infectie met EEEV. De incubatieperiode van EEE is meestal 5 tot 10 dagen. In Noord-Amerika treden gemiddeld 7 EEE-gevallen per jaar op, met name bij kinderen jonger dan 15 jaar en volwassenen ouder dan 55 jaar. De ratio tussen asymptomatische infecties of infecties met aspecifieke ziekteverschijnselen versus infecties met neurologische symptomen is globaal 17:1 in kinderen (1:1 in kinderen < 1 jaar) en 40:1 in volwassenen. De mortaliteit van EEE (bij optreden van neurologische verschijnselen) is 30 tot 70 procent. Mensen met neurologische verschijnselen die de infectie overleven, blijven vaak permanent last houden van de nasleep van de ziekte. Ernstige infecties en sterfte zijn gevonden bij laboratoriummedewerkers die niet de juiste persoonlijke beschermingsmaatregelen in acht namen. Daarom dient werk aan deze virussen uitsluitend in laboratoria met isolatieniveau 3 te geschied
EEEV overleeft niet buiten de gastheer, dus persisteert niet in de omgeving.
EEEV is gevoelig voor de meeste gebruikelijke desinfectantia (Natrium Hypochloriet, Halamid, formaline, ethanol, glutaaraldehyde). Het virus is gevoelig voor vochtige en droge verhitting en voor droogte.
Terug naar het begin van dit artikel
Klinisch beeld
Na een incubatietijd van 5 tot 10 dagen beginnen de klinische verschijnselen van een EEE-infectie bij paarden meestal met koorts, gebrek aan eetlust en depressie. In de ernstige gevallen volgt een ontsteking van hersenen, ruggenmerg en hersenvliezen. Humaan zijn EEE-infecties gekenmerkt door het acute optreden, hoofdpijn met koorts en aseptische meningitis. In ernstige gevallen is er sprake van hoge koorts, hevige hoofdpijn, trillingen, spasmen, krampen en verlammingen met tot 60 procent sterfte. Bij paarden zijn de meest kenmerkende neurologische verschijnselen excitatie, blindheid, ataxie, ernstige mentale depressie, verlamming, krampen en sterfte. EEE staat in de differentiaal diagnose indien niet gevaccineerde paarden de karakteristieke slaperigheid vertonen gedurende de zomer in gematigde klimaatzones of gedurende het regenseizoen in tropische en subtropische regio’s. Echter: andere door muggen overgebrachte ziekten zoals West Nile Fever kunnen ongeveer dezelfde klinische verschijnselen geven.
Morbiditeit/mortaliteit
In 1933 werd EEEV voor het eerst geisoleerd uit besmette paarden in Virginia en New Jersey. In 1947 stierven 12.000 paarden in Louisiana ten gevolge van een EEE-epidemie. Sinds veel paarden gevaccineerd worden tegen EEE is de morbiditeit en mortaliteit aanzienlijk gedaald en komt het meestal slechts nog in individuele gevallen voor. Soms treden nog EEE-epidemieën op in de zuidelijke staten van de USA, waar het vectorseizoen relatief te lang kan duren ten opzichte van de kortdurende immuniteit na vaccinatie. Bij paarden met neurologische verschijnselen is de case fatality ratio bij EEE zeer hoog (tot 90 procent). Humaan is de case fatality ratio bij neurologische verschijnselen ten gevolge van EEE 30 tot 60 procent.
Uitscheiding van de kiem
Bij paarden en mensen is er geen sprake van uitscheiding van de kiem. Besmetting vindt plaats door muggen die bij viremische vogels hun bloedmaal hebben opgenomen. De viremie in vogels duurt 2 tot 5 dagen. Muggen blijven echter levenslang reservoir, en verticale transmissie naar muggeneieren is mogelijk. Het virus overwintert waarschijnlijk in (eieren van) muggen en in vogels, knaagdieren, vleermuizen, reptielen en amfibieën.
Differentiaaldiagnostiek
Omdat geen enkel verschijnsel specifiek c.q. pathognomonisch is, is zonder diagnostische testen geen onderscheid te maken met een aantal andere ziekten zoals Venezuelan en Western Equine Encephalomyelitis, West Nile Fever, Afrikaanse Paardenpest, Rabiës, Infectieuze Anemie, Equine Herpesvirus Myeloencephalopathie (EHM), in Amerika Equine Protozoal Myeloencephalitis (EPM), vermineuze encephalopathie, neuroborreliose, cervicale vertebrale stenose, diverse vergiftigingen, Botulisme, Leverkolder en trauma.
Terug naar het begin van dit artikel
Pathologie
Grove pathologische laesies ontbreken vaak bij paarden. Hoogstens zijn congesties van de hersenen en meningen te zien. Eventueel worden puntbloedingen door trauma waargenomen. Microscopische laesies worden gewoonlijk wel aangetroffen in het gehele zenuwstelsel en zijn van diagnostische waarde. Er is een wijdverspreide ontstekingsreactie in de grijze hersensubstantie. De laesies komen meer voor in de grijze stof dan in de witte stof en met name in de cerebrale cortex, thalamus en hypothalamus. Degeneratie en necrose van neuronen met gliosis en infiltratie van ontstekingscellen treedt vaak op. Perivasculaire ophopingen van lymfocyten en neutrofielen zijn te zien. De mate van voorkomen van laesies hangt af van de ernst van de infectie en de duur van de neurologische verschijnselen. EEE kan via immunohistochemie, maar ook via in situ hybridisatie of RT-PCR rechtstreeks op hersenmateriaal worden aangetoond.
Isolatie van de kiem
Het EEE-virus kan worden geïsoleerd uit de hersenen van gestorven paarden als zij korter dan 5 dagen geleden zijn begonnen met het vertonen van klinische verschijnselen. Ook uit andere weefsels, zoals lever of milt, kan het virus in de eerste vijf dagen na infectie geïsoleerd worden. EEE-virus kan ook bij aanwezigheid van een hoge titer aan antistoffen (door eerdere vaccinaties of infecties) worden geïsoleerd. Diverse kweeksystemen zijn geschikt (Vero, BHK-21, RK-13, geëmbryoneerde kippeneieren). Materiaal moet binnen 48 uur na gekoelde bewaring en transport worden onderzocht. Is dit niet mogelijk dan dient het materiaal te worden ingevroren en onder droog ijs te worden verzonden. Vriezen verkleint echter de kans op virusisolatie aanzienlijk. Een complete set materiaal, bestaande uit hersenen, lever en milt, moet worden verstuurd. Er bestaat een groot gevaar op humane infectie bij de isolatie van virus uit besmette vogels door aërosolvorming van uiterst infectieus virus. EEEV in muggen en weefsels kan worden aangetoond met een RT-PCR. In landen zonder de faciliteiten voor virusisolatie of PCR kan ook een ELISA worden gebruikt voor het vaststellen van de besmettingsgraad in muggen.
Serologie
Voor het aantonen van antistoffen zijn de CBR, de haemagglutinatie reductie test (HI-test), een IgM capture ELISA en een Plaque Reductie Neutralisatie Test (PRN-test) beschikbaar. De IgM capture ELISA kan naast serum ook op CSF uitgevoerd worden, maar dit geeft bij paarden minder consistente resultaten dan in geval van serum (dit in tegenstelling tot de humane diagnostiek). EEE-infecties kunnen ook worden aangetoond in gepaarde sera, genomen met 10 tot 14 dagen tussentijd. Een viervoudige titerstijging is dan vereist voor het stellen van de diagnose. Meestal hebben paarden met klinische verschijnselen zeer hoge titers tegen EEEV. Detectie van IgM met een capture enzyme ELISA geeft een snelle voorlopige diagnose bij een acute infectie. De PRN-test of de combinatie van de PRN-test met de HI-test zijn het betrouwbaarst voor het aantonen van antistoffen. De CBR toont antistoffen tegen EEEV later aan en de reactie blijft niet positief; daardoor is de CBR minder bruikbaar voor de serologische diagnostiek. In de CBR- en HI testen kunnen antilichamen tegen EEEV en WEEV kruisreacties vertonen. De PRN-test is het meest specifiek en kan gebruikt worden om onderscheid te maken tussen EEE- en WEE-virus.
Terug naar het begin van dit artikel
Nederland
EEE komt in Nederland niet voor.
Andere landen
Europa
EEE (en WEE) komen niet voor in Europa.
Landen buiten Europa
EEE komt voor in Canada (Quebec en Ontario), USA (Texas, staten ten oosten van Mississippi), de Caribische Eilanden, Mexico en Midden- en Zuid-Amerika. In 2017 werden de eerste gevallen van EEE in Suriname gerapporteerd. Tan et al analyseerden de genomen van 433 EEEV stammen verzameld in de USA tussen 1934 en 2014. Hieruit bleek dat EEV betrekkelijk langzaam evolueert en endemisch is in Florida en dat het virus met name vanuit Florida zich verspreidt naar andere staten.
Voor gedetailleerde informatie over de verspreiding zie: OIE: World Animal Health Situation en OIE bulletin (www.oie.int).
Terug naar het begin van dit artikel
Vaccinatie
Er zijn in de USA diverse goede vaccins voor paarden beschikbaar. Met een goed vaccinatieschema is EEE bij paarden volledig te voorkomen. Fokmerries moeten een maand voor het veulenen worden gevaccineerd om een goede overdracht van maternale antistoffen te realiseren. Veulens uit goed gevaccineerde merries moeten vervolgens op een leeftijd van 6, 7, en 9 maanden gevaccineerd worden. Indien de merrie tijdens de dracht niet is gevaccineerd moet het veulen gevaccineerd worden op 4, 5 en 7 maanden (basis immunisatie). Vervolgens moeten in endemische gebieden paarden na de veulen vaccinaties drie keer paar jaar gevaccineerd worden met intervallen van 4 maanden. Vanaf een leeftijd van vier jaar kan vervolgens volstaan worden met twee keer per jaar vaccineren. De meeste vaccins zijn geïnactiveerde volvirusvaccins die tijdig moeten worden toegediend (starten met een basisimmunisatie van drie vaccinaties). Vaak betreft het combinatievaccins voor EEE, WEE en VEE. Er zijn geen humane vaccins geregistreerd. Wel worden er in de USA bepaalde groepen militairen en laboratoriumpersoneel gevaccineerd. Deze vaccins geven na diverse booster injecties een acceptabele antistof respons gecorreleerd met bescherming. Ook wordt er hard gewerkt aan nieuwe vaccins zoals MVA vector vaccins en DNA vaccins, waarbij goede bescherming in muizen gerapporteerd wordt. Recent werd een fase II studie gerapporteerd met een klassiek geinactiveerd EEE vaccin. Hierbij vertoonde bijna 60% van de vrijwilligers een of meer bijwerkingen, maar de conclusie van de studie was toch dat het vaccin voldoende veilig en immunogeen was om de volgende stap naar registratie te kunnen maken. Zie verder onderstaande tabel voor commerciele vaccins voor de diverse veroorzakers van equine encephalomyelitis bij paarden.
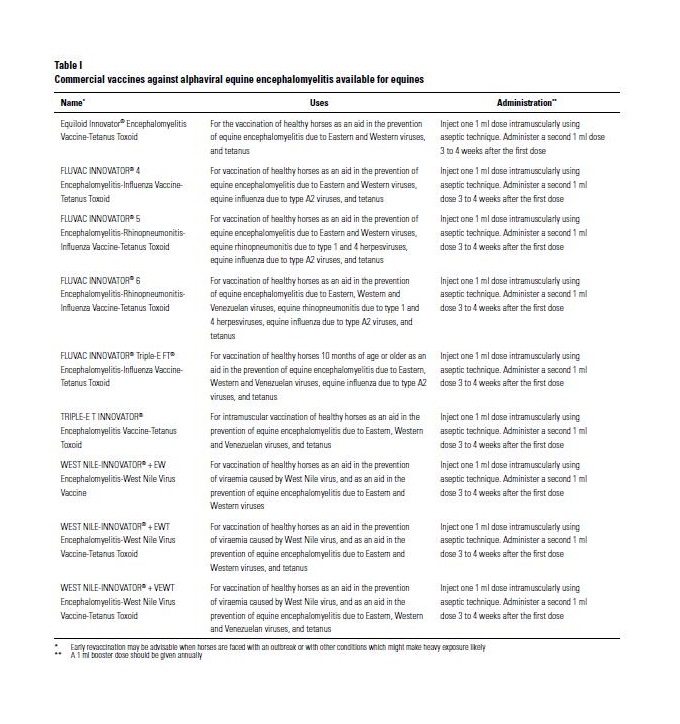
Antibiotica/therapie
Er is geen specifieke behandeling. De behandeling van neurologische patiënten bestaat uit ondersteunende therapie met goede verzorging, NSAIDs, zo nodig infusen en electrolyten en convulsie-remmers. Er zijn geen specifieke virostatica met een bewezen werking tegen EEE-infecties bij het paard, al werden door Hu et al. in muizen veelbelovende resultaten gerapporteerd voor sorafenib. Dit voor andere doeleinden door de FDA goedgekeurde geneesmiddel bleek zowel de replicatie van VEEV als EEEV effectief te remmen, waarschijnlijk door het remmen van de translatie door defosforylering van verschillende essentiele virale eiwitten. Recent onderzoek heeft aangetoond dat enkele neutraliserende monoclonale antistoffen opgewekt in muizen 100% bescherming gaven in twee verschillende doses en dat ook geen virus in de hersenen van deze muizen aangetoond kon worden op 14 dagen na infectie. Deze antistoffen bieden potentieel voor immunotherapie bij EEEV of WEEV infecties.
Overige maatregelen
Bescherming van paarden
Besmette paarden zijn niet direct infectieus voor de omgeving. Paardenvliegendekens geïmpregneerd met permetrin kunnen de infectieoverdracht door muggen beperken. Ventilatoren in de stallen verlagen de muggendruk, evenals het bespuiten van de stalmuren met insecticiden. Opstallen kan het beste plaatsvinden voordat de schemering invalt en gedurende de nacht. De muggenactiviteit is namelijk het hoogst tussen zonsondergang en zonsopgang.
Algemene maatregelen
De hoogste veiligheidseisen met betrekking tot laboratoriummedewerkers zijn geboden (niveau 3 biosecuriteit). Naast vaccinaties van eerder genoemde categorieën personen zijn quarantainemaatregelen nodig, samen met een onderzoek naar de verspreiding. Voor dit laatste is onderzoek nodig van zowel de muggen als het bloed van de paarden in de omgeving van de uitbraak.
Maatregelen in kader volksgezondheid
Communicatie en publieksvoorlichting zijn van groot belang. Deze communicatie dient zich te richten op algemene maatregelen ter voorkoming van vector-overdraagbare (in dit geval door muggen overdraagbare) ziekten. Deze adviezen zullen met name betrekking moeten hebben op het reduceren van muggenpopulaties door het weghalen van alle bronnen met stilstaand water in en om het huis, het dragen van bedekkende kleding, het gebruik van repellents zoals Deet en eventueel het gebruik van muskietennetten/klamboes en het toepassen van insecticiden in de directe omgeving (voor zover toegestaan binnen de Nederlandse wetgeving).
In de USA heeft men daar het volgende ezelsbruggetje van de 5 Ds voor bedacht:
- Dusk/Dawn (vermijd in de zomerperiode/vectorseizoen outdoor activiteiten bij zonsopgang en zonsondergang)
- Dress (draag lange broeken en shirts met lange mouwen)
- DEET (gebruik DEET op de onbedekte huiddelen)
- Drain (verwijder alle containers/emmers etc. met stilstaand water)
- Doors (zorg ervoor dat deuren en ramen goed sluiten en dat muggengaas/horren intact zijn).
Terug naar het begin van dit artikel
Bedrijfshygiëne/insleeppreventie
Muggenbestrijding is in de praktijk moeilijk uitvoerbaar. Een aantal praktisch uitvoerbare (preventieve) maatregelen in de directe omgeving van mens en dier is behandeld in hoofdstuk 5.
Vaccinatie
Voor paarden zijn vaccins beschikbaar (zie onder Aanpak besmette bedrijven/vaccinatie). In hoeverre deze in Nederland zullen mogen worden toegepast is onduidelijk. Daarnaast wordt muggenbestrijding en het gebruik van muggendekens, DEET, enzovoorts, aanbevolen.
Terug naar het begin van dit artikel
Regelgeving
Nederlands recht
EEE is in Nederland volgens de AHReen aangifteplichtige ziekte. EEE valt onder de virale paarden-encefalomyelitiden.
Europees recht
EEE is een meldingsplichtige ziekte volgens de Europese diergezondheidsverordening (Animal Health Regulation AHR). Vanaf 21 april 2021 valt het voorkomen en bestrijden van dierziekten namelijk onder deze verordening. EEV valt in categorie E.
De dierziekten in de Europese Diergezondheidsverordening zijn ingedeeld in de vijf categorieën A, B, C, D en E. Voor alle ziekten uit deze categorieën geldt een meldingsplicht, voor de ziekten uit categorieën A en B geldt daarnaast ook een bestrijdingsplicht.
- Dierziekten van categorie A zijn ziekten die niet in de Europese Unie voorkomen en die lidstaten meteen moeten uitroeien. Bijvoorbeeld mond-en-klauwzeer en varkenspest. Lidstaten moeten deze ziekten snel opsporen, direct bestrijden en besmette bedrijven en de directe omgeving afsluiten.
- Dierziekten van categorie B zijn ziekten die de Europese Unie wil uitroeien. Bijvoorbeeld tuberculose bij koeien, stieren en buffels. Lidstaten moeten deze ziekten daarom verplicht bestrijden. Lidstaten waar de ziekte niet voorkomt moeten maatregelen nemen om vrij te blijven van de ziekte.
- Dierziekten van categorie C zijn ziekten die minder besmettelijk zijn en die de Europese Unie wil indammen. Bijvoorbeeld de ziekte van Aujesky bij varkens en koeiengriep bij runderen. Lidstaten bepalen zelf of ze de ziekte willen uitroeien en of ze bij een uitbraak bedrijven afsluiten om verdere verspreiding te voorkomen.
- Dierziekten van categorie D zijn dierziekten die zich via internationale handelaren, vervoerders of reizigers verspreiden en die de Europese Unie wil indammen. Bijvoorbeeld abortus blauw bij varkens en verkoudheid (mycoplasma) bij kippen. Landen moeten voldoen aan Europese regels voor vervoer van en naar de EU en erbinnen.
- Dierziekten van categorie E zijn dierziekten die in de gaten gehouden moeten worden. Bijvoorbeeld Q-koorts bij geiten en paratuberculose bij runderen. Lidstaten moeten zich houden aan Europese regels om deze ziekten te melden.
EEEV komt voor op de lijst van ‘goederen’ die zijn opgenomen in bijlage I bij Besluit 1999/193/GBVB van de Raad van 9 maart 1999 tot wijziging van Besluit 94/942/GBVB betreffende het Gemeenschappelijk optreden. Dit is door de Raad vastgesteld op grond van artikel J.3 van het Verdrag betreffende de Europese Unie, ten aanzien van de controle op de uitvoer van goederen voor tweeërlei gebruik.
Internationaal
Het verkeer van paarden binnen de EU en de invoer van paarden vanuit derde landen is geregeld in Richtlijn 90/426/EEG van de Raad van 26 juni 1990 tot vaststelling van veterinairrechtelijke voorschriften voor het verkeer van paardachtigen en de invoer van paardachtigen uit derde landen. Hierin staan alleen specifieke bepalingen voor Afrikaanse paardenpest, VEE, Dourine en kwade droes genoemd, zoals hieronder aangegeven. Wel kunnen volgens artikel 13 lid 2b aanvullende waarborgen geëist worden voor ziekten die in de Gemeenschap exotisch zijn.
Artikel 13
1. De paardachtigen moeten afkomstig zijn uit derde landen:
a) die vrij zijn van paardenpest;
b) die sedert twee jaar vrij zijn van Venezolaanse paardenencefalomyelitis (VEE);
c) die sedert zes maanden vrij zijn van dourine en van kwade droes.
2. Volgens de procedure van artikel 24 kan de Commissie
a) beslissen dat lid 1 slechts voor een gedeelte van het grondgebied van een derde land geldt. In geval van regionalisering van de vereisten ten aanzien van paardenpest dienen ten minste de in artikel 5, leden 2 en 3, genoemde maatregelen in acht te worden genomen;
b) aanvullende waarborgen eisen voor ziekten die in de Gemeenschap exotisch zijn
Terug naar het begin van dit artikel
Websites
Literatuur
- Aréchiga-Ceballos N, Aguilar-Setién A. Alphaviral equine encephalomyelitis (Easter, Western and Venezuelan). Rev Sci Tech Off Int Epiz 2015; 34 (2): 491-501
- Bauer RW, Gill MS, Poston RP, Kim DY. Naturally occurring eastern equine encephalitis in a Hampshire rel="noopener noreferrer" wether. J Vet Diagn Invest. 2005;17:281-5.
- Calisher CH. Medically important arboviruses of the United States and Canada. Clin Microbiol Rev. 1994;7:89-116.
- Centers for Disease Control and Prevention (CDC). Information on arboviral encephalitides [online]. CDC; rel="noopener noreferrer" 2005 Nov. Available at: https://www.cdc.gov/ncezid/dvbd/. Accessed 4 Apr. 2008.
- Cupp EW, Zhang D, Yue X, Cupp MS, Guyer C, Sprenger TR, Unnasch TR. Identification of reptilian and amphibian blood meals from mosquitoes in an eastern equine encephalomyelitis virus focus in central Alabama. Am J Trop Med Hyg. 2004;71:272-6.
- Del Piero F, Wilkins PA, Dubovi EJ, Biolatti B, Cantile C. Clinical, pathologic, immunohistochemical, and virologic findings of eastern equine encephalomyelitis in two horses. Vet Pathol. 2001;38:451-6.
- Dupuy LC, Richards MJ, Livingston BD, Hannaman D, Schmaljohn CS. A Multiagent Alphavirus DNA Vaccine Delivered by Intramuscular Electroporation Elicits Robust and Durable Virus-Specific Immune Responses in Mice and Rabbits and Completely Protects Mice against Lethal Venezuelan, Western, and Eastern Equine Encephalitis Virus Aerosol Challenges. J Immunol Res. 2018 Jun 3;2018:8521060.
- Garner G, Saville P, Fediaevsky A. Manual for the Recognition of Exotic Diseases of Livestock: A Reference Guide for Animal Health Staff [online]. Food and Agriculture Organization of the United Nations [FAO]; 2004. Equine viral encephalomyelitis.
- Guy JS, Barnes HJ, Ficken MD, Smith LG, Emory WH, Wages DP. Decreased egg production in turkeys experimentally infected with eastern equine encephalitis virus or Highlands J virus. Avian Dis. 1994;38:563-71.
- Guy JS, Barnes HJ, Smith LG Experimental infection of young broiler chickens with eastern equine encephalitis virus and Highlands J virus. Avian Dis. 1994;38:572-82.
- Hu WG, Steigerwald R, Kalla M, Volkmann A, Noll D, Nagata LP. Protective efficacy of monovalent and trivalent recombinant MVA-based vaccines against three encephalitic alphaviruses. Vaccine. 2018 Aug 16;36(34):5194-5203.
- Long MT. West Nile Virus and Equine Encephalitis Viruses – New Perspectives. Vet Clin Equine 2014; 30: 523-542.
- Lundberg L, Brahms A, Hooper I, Carey B, Lin SC, Dahal B, Narayanan A, Kehn-Hall K. Repurposed FDA-Approved drug sorafenib reduces replication of Venezuelan equine encephalitis virus and other alphaviruses. Antiviral Res. 2018 Sep;157:57-67
- Public Health Agency of Canada, Office of Laboratory Security. Material Safety Data Sheet: Venezuelan equine encephalitis virus, Eastern equine encephalitis virus [online]. Office of Laboratory Security; 2001 Jan.
- Pursell AR, Mitchell FE, Siebold HR. Naturally occurring and experimentally induced eastern encephalomyelitis in calves. J Am Vet Med Assoc. 1976;169:1101-3.
- Pursell AR, Peckham JC, Cole JR Jr, Stewart WC, Mitchell FE. Naturally occurring and artificially induced eastern encephalomyelitis in pigs. J Am Vet Med Assoc. 1972;161:1143-7.
- Schmitt SM, Cooley TM, Fitzgerald SD, Bolin SR, Lim A, Schaefer SM, Kiupel M, Maes RK, Hogle SA, O'Brien DJ. An outbreak of Eastern equine encephalitis virus in free-ranging white-tailed deer in Michigan. J Wildl Dis. 2007;43:635-44.
- Tan Y, Tsan-Yuk Lam T, Heberlein-Larson LA, Smole SC, Auguste AJ, Hennigan S, Halpin RA, Fedorova N, Puri V, Stockwell TB, Shilts MH, Andreadis T, Armstrong PM, Tesh RB, Weaver SC, Unnasch TR, Ciota AT, Kramer LD, Das SR. Large scale complete genome sequencing and phylodynamic analysis of eastern equine encephalitis virus reveal source-sink transmission dynamics in the United States. J Virol. 2018 Apr 4.
- Tully TN Jr, Shane SM, Poston RP, England JJ, Vice CC, Cho DY, Panigrahy B. Eastern equine encephalitis in a flock of emus (Dromaius novaehollandiae). Avian Dis. 1992 Jul-Sep;36(3):808-12.
- Williams SM, Fulton RM, Patterson JS, Reed WM. Diagnosis of eastern equine encephalitis by immunohistochemistry in two flocks of Michigan ring-neck pheasants. Avian Dis. 2000;44:1012-6.
- World Organization for Animal Health [OIE] . Manual of diagnostic tests and vaccines for terrestrial animals [online]. Paris: OIE; 2008. Equine encephalomyelitis rel="noopener noreferrer" (eastern and western). Available at: http://www.oie.int/fileadmin/Home/eng/Health_standards/tahm/A_index.htm
Terug naar het begin van dit artikel