- Home
- Dierziektes
- Q-fever
Q-fever
Q-fever, ook wel Q-koorts genoemd, is een wereldwijd voorkomende infectie bij mens en dier. Herkauwers worden beschouwd als de belangrijkste besmettingsbron voor de mens. Abortus is het belangrijkste klinische verschijnsel bij kleine herkauwers en runderen. De verwekker van Q-fever is de obligaat intracellulaire Gram-negatieve bacterie Coxiella burnetii. Q-fever bij kleine herkauwers is een meldingsplichtige ziekte. Een afwijkend aantal abortussen bij schaap en geit is het meldcriterium. Elke verdenking van de ziekte dient te worden gemeld bij de NVWA.
In december 2021 heeft overleg plaatsgevonden met de NVWA aangaande de meldplicht rondom Q-fever bij dieren. Op basis van de Animal Health Regulation ((AHR) in werking getreden op 21 april 2021) waren er vragen over de invulling hiervan met betrekking tot Q-fever.
De aandoening is op basis van de AHR gecategoriseerd als E-ziekte. Dit betekent dat positieve bevindingen worden gerapporteerd aan de NVWA (immuunhistochemie, PCR en ELISA). Dit betreft niet alleen bevindingen in monsters van schapen en geiten, maar ook runderen. Dit dient elk kwartaal en anoniem te gebeuren. In Nederland geldt voor schapen en geiten aanvullend een aangifteplicht (zie www.nvwa.nl/onderwerpen/q-koorts) voor een afwijkend aantal abortussen. Daarnaast is de tankmelkmonitoring verplicht voor Nederlandse melkschapen- en melkgeitenbedrijven met meer dan vijftig dieren. Wanneer bij tankmelkonderzoek (PCR) op melkschapen-en melkgeitenbedrijven met meer dan vijftig dieren C. burnetii wordt aangetoond wordt het monster ter confirmatie aan WBVR aangeboden. Indien het monster ook daar positief wordt bevonden zal een ambtelijk monster door de NVWA worden genomen. Op basis van de uitslag van het ambtelijk monster zal het bedrijf een status (besmet of niet) toegekend krijgen. Vaccinatie tegen Q-koorts is in Nederland verplicht voor melkschapen- en melkgeitenbedrijven met meer dan vijftig dieren, schapen en geiten op bedrijven met een publieksfunctie en schapen en geiten die naar keuringen en/of shows gaan.
In 2021 heeft het ministerie van LNV het beleidsdraaiboek bestrijding Q-koorts aangepast. Dit draaiboek is te vinden via de website www.rijksoverheid.nl.
Veterinair kennisdossier Q-fever
- Verschijnselen
- Diagnose
- Prevalentie
- Aanpak besmette bedrijven
- Preventie
- Regelgeving
- Websites en literatuur
De kiem
C. burnetii is een obligaat intracellulaire, Gram-negatieve bacterie. De kiem behoort tot de orde van de Legionellae, in de familie Coxiellaceae, waarvan C. burnetii het enige species is. Eerder werd de kiem ingedeeld bij de Rickettsiae. De bacterie wordt in twee vormen aangetroffen: een small-cell-variant (SCV) en een large-cell-variant (LCV). Deze vormen zijn te onderscheiden met elektronenmicroscopie. De SCV is zeer infectieus. De SCV wordt bij entree in een gastheer (dier of mens) gefagocyteerd door macrofagen, en vormt zich vervolgens in de fagocyt om tot LCV. Als LCV vermeerdert de kiem zich in de fagocyten, en blijft daar persistent aanwezig.
C. burnetii heeft twee antigene fasen: fase I en fase II. Wanneer de bacterie direct uit een dier of mens wordt onderzocht, is deze in fase I, wanneer de bacterie enkele malen gekweekt is op celcultuur of bebroede kippeneieren, is deze in fase II. Deze antigene variatie heeft zijn oorsprong in een verandering in de LPS-laag (lipo-polysaccharide-laag) van de bacterie. In fase I is de LPS-laag compleet en zorgt deze er onder meer voor dat immuunglobulinen van de gastheer gehinderd worden bij het binden aan de oppervlakte-eiwitten van de bacterie, daarmee een effectieve afweerreactie verstorend. In fase I is C. burnetii zeer infectieus en virulent. In fase II heeft het LPS een andere suikersamenstelling en is het LPS korter. Hierdoor krijgen immuunglobulinen de kans de bacterie te naderen en onschadelijk te maken. Deze variatie in antigene fasen (fase I en fase II) is analoog aan "smooth"- en "rough"-varianten van andere Gram-negatieve bacteriën. Dit is van belang in de diagnostiek en de vaccinbereiding. C. burnetii-isolaten zijn genetisch sterk homogeen, maar met restrictie enzym technieken kunnen wel verschillende stammen onderscheiden worden.
Gevoelige diersoorten
C. burnetii is in veel wilde en gedomesticeerde dieren gevonden, waaronder runderen, schapen, geiten, honden, katten, ratten en ook bij diverse vogels, allerlei insecten en teken. Gedomesticeerde herkauwers worden als belangrijkste reservoir gezien.
Volksgezondheid
Het eerste beschreven geval van Q-fever betrof een uitbraak van koorts onder slachthuispersoneel in Queensland (Australië) in 1935 en is nader onderzocht door Burnet, waardoor de ziekteverwekker mede zijn naam kreeg. Het reservoir voor de mens is de dierenwereld. In het algemeen worden schapen, geiten en runderen als de belangrijkste bron voor infecties van de mens gezien. Ook katten, honden en knaagdieren zijn mogelijke bronnen voor humane infecties. Infecties van mens op mens zijn zeldzaam. De belangrijkste porte d'entree bij de mens is het respiratoire slijmvlies of de conjunctiva, en waarschijnlijk is ook het intestinale slijmvlies een mogelijke route. Na opname volgt een hematogene verspreiding en een systemische infectie. Bij de mens is de infectie meestal zelflimiterend. Bij dieren kan de bacterie waarschijnlijk in het baarmoederslijmvlies en in de melkklieren persisteren. Waarschijnlijk is dat bij mensen ook het geval. C. burnetii is ook bij mensen in placenta en moedermelk aangetoond.
De ziekteverschijnselen bij de mens zijn divers. Een groot deel van de infecties gaat symptoomloos voorbij. Wanneer er wel verschijnselen optreden, bestaan ze in de acute fase uit griepachtige symptomen: langdurig (7-10 dagen) hoge koorts, hoofdpijn, spierpijn, geen eetlust, misselijkheid, braken, diarree, hoesten en pijn op de borst. Een atypische pneumonie of leverontsteking wordt regelmatig gezien. De incubatietijd is 2-4 weken, soms tot 6 weken. In een goed gedocumenteerde uitbraak in Zwitserland leidde een uitbraak tot hospitalisatie van 2% van de besmette mensen. In de periode 2007-2009 lag dat percentage in Nederland veel hoger. Wanneer de infectie chronisch verloopt, kan een endocarditis ontstaan. Deze kan jaren na de oorspronkelijke infectie nog manifest worden. In Zuid-Frankrijk bijvoorbeeld wordt 5-8% van de endocarditisgevallen door C. burnetii veroorzaakt. In internationale literatuur is er een relatie beschreven tussen Q-fever-infectie en abortus of doodgeboren kinderen. Tijdens de Q-fever-uitbraak in Nederland, tussen 2007-2010, zijn geen aanwijzingen gevonden voor een relatie tussen Q-fever-infectie en miskramen/doodgeboren kinderen. Ook chronische vermoeidheid wordt als symptoom gezien. Meestal herstellen mensen met Q-fever, maar wanneer de infectie chronisch is geworden, kan sterfte optreden (1-11%). In de laatste jaren zijn veel publicaties verschenen over chronische infecties met Q-koorts bij mensen (bijvoorbeeld in geval van prothesen) en het chronisch vermoeidheidssyndroom.
Nederland
Tot 2007 werden er in Nederland jaarlijks ongeveer 5-20 humane gevallen van Q-koorts gemeld. In 2007 trad een stijging op van het aantal humane gevallen op, met name in de regio rond Herpen (Noord-Brabant). In 2008 en 2009 steeg het aantal humane gevallen nog sterker, ook in andere delen van ons land. In 2008 was het aantal humane gevallen ongeveer duizend. In 2009 bedroeg het aantal bijna 2400. In 2009/2010 zijn uitgebreide maatregelen (o.a. vaccinatie, ruimen van drachtige dieren, hygiënemaatregelen) getroffen om de uitscheiding van de bacterie door schapen en geiten te verminderen. Dit pakket aan maatregelen heeft geleid tot verminderde contaminatie van de omgeving en zodoende tot beduidend minder humane ziektegevallen in 2010, 2011, 2012, 2013 en de eerste helft van 2014. In 2017 werd Q- fever vastgesteld bij drie mensen uit één Nederlands gezin. Er is brontracering uitgevoerd naar aanleiding van dit kleine cluster van patiënten. Ondanks uitgebreid onderzoek is de bron niet gevonden.
In 2018 is in een persbericht gemeld dat het aantal humane sterfgevallen in Nederland ten gevolge van chronische Q-fever hoger ligt dan aanvankelijk werd gedacht. In juni 2019 werd via het Signaleringsoverleg Zoönosen melding gemaakt van een mogelijk cluster van drie patiënten in de GGD regio West-Brabant en in totaal werd in 2019 door het RIVM melding gemaakt van 19 patiënten met Q-koorts. In 2021 heeft het RIVM melding gemaakt van zeven patiënten met Q-fever. In 2022 heeft het RIVM melding gemaakt van tien patiënten met Q-fever. In 2023 is via het RIVM melding gemaakt van zes humane patiënten (tot 11 oktober 2023). Ondanks dat het aantal besmettingen in lijn is met de periode voor 2007 en er diverse maatregelen worden genomen om uitscheiding door bepaalde groepen kleine herkauwers te monitoren en te voorkomen, is er nog steeds veel aandacht voor Q-fever in Nederland.
Buitenland
Via Promed zijn in 2018 uitbraken van Q-fever in Australië, Chili en Spanje gemeld. De uitbraak in Spanje betreft patiënten werkzaam op een afvalverwerkingsstation. Mogelijk zijn placenta’s van geïnfecteerde dieren die als afval zijn aangeboden aan dit station de oorzaak van deze uitbraak. Overigens is ook in 2011 een uitbraak op een afvalverwerkingsstation in Spanje beschreven. In 2019 is via Promed melding gemaakt van Q-fever bij Britse militairen die in Afghanistan gelegerd waren. Daarnaast maakte Zwitserland via Promed melding van meerdere patiënten met pneumonie ten gevolge van Q-fever in de Ticino Maggia Valley. In 2020 is via Promed melding gemaakt van een uitbraak van Q-fever in Bulgarije. Via Promed is door Australië gewezen op het belang van vaccinatie van “people at risk”, vanwege hun grotere risico op infectie vanwege contacten met risicodieren. In 2021 zijn diverse Australische publicaties verschenen die het belang van vaccinatie van people at risk in Australië onderschrijven.
Via Promed is in 2021 opnieuw melding gemaakt van een uitbraak op een afvalverwerkingsstation in Spanje. In dit geval betrof het ten minste drie patiënten. Chili maakte melding van een jonge landbouwhuisdieren-dierenarts die Q-fever zou hebben gekregen. In een later stadium werd de diagnose herzien en bleek het te gaan om psittacose. Tot slot, in Duitsland werd melding gemaakt van ten minste vijftien patiënten onder laboratorium personeel dat de infectie had opgedaan via C. burnetii uitscheidende schapen. In Duitsland werd later melding gemaakt van een infectie onder laboratoriumdieren. In 2022 werd via Promed melding gemaakt van het voorkomen van Q-fever in Australië, Rusland, Spanje, Kroatië en Argentinië. In 2023 werd het voorkomen van Q-fever via Promed gemeld in India, Bosnië, Kroatië, Duitsland, Bulgarije, Spanje, Zuid-Korea en Roemenië.
Overleving
De small-cell-variant van de bacterie is zeer resistent voor chemische invloeden, uitdroging en temperatuur, en wordt soms ook wel "spore" genoemd. Deze vorm is zeer stabiel in aërosolen. Zo kan de kiem via stof verspreid worden.Desinfectie
C. burnetii is bestand tegen veel desinfectantia. Werkzame desinfecteermiddelen moeten gedurende 24-48 uur worden toegepast. Werkzame desinfectantia zijn: ethanol, gasvormig formaldehyde, 5% peroxide en 0.05% hypochloriet. Mest kan behandeld worden met calciumcyanide (0.6%) gedurende één week. Compostering van mest is ook effectief gebleken. In de praktijk betekent dit dat een effectieve, praktisch uitvoerbare desinfectie op rundveebedrijven niet of nauwelijks bestaat.
Verschijnselen van Q-fever
Klinische verschijnselen
Achtergronden
Indien er klinische verschijnselen optreden bij schapen, geiten of runderen, is abortus in een gevorderd stadium van de dracht het belangrijkste symptoom. In dit stadium is sprake van de grootste besmettelijkheid, ook voor de mens. Naast abortus worden doodgeboorte, aan de nageboorte staan, baarmoederontsteking en onvruchtbaarheid als klinische verschijnselen genoemd, maar tot nu toe is dit niet goed onderbouwd. Placentitis is het meest karakteristieke kenmerk van Q-fever. Soms kan het exsudaat roodbruin van kleur zijn. Kleine stolsels en vaatwandontsteking kunnen gezien worden bij histologisch onderzoek. In diverse landen is onderzoek gedaan naar het voorkomen van C. burnetii bij runderen met vruchtbaarheidsproblemen. In Italië werden sera van 650 runderen die hadden verworpen, onderzocht op afweerstoffen tegen C. burnetii (ELISA). Bij 600 at random verzamelde sera werd hetzelfde onderzoek gedaan. De percentages seropositieve dieren waren significant verschillend tussen beide groepen en bedroegen respectievelijk 45% en 22%. De hoogste prevalenties werden gezien bij runderen die in de herfst aborteerden en/of hoogdrachtig waren. In een ander Italiaans onderzoek zijn 138 geaborteerde runderfoetussen onderzocht, waarbij 12% PCR positief was.
In een Japans onderzoek zijn 61 uterusswabs van melkkoeien met vruchtbaarheidsproblemen onderzocht op de aanwezigheid van C. burnetii: bij 21% werd de kiem aangetoond met een PCR. Dit suggereert een hoge prevalentie van de kiem bij Japans melkvee met vruchtbaarheidsproblemen. Een vergelijkbaar resultaat is ook gevonden in een serologisch onderzoek met behulp van een CBR-test. Runderen met vruchtbaarheidsproblemen waren vaker CBR-positief dan runderen met een normale vruchtbaarheid. In een onderzoek van Tainturier is C. burnetii als oorzaak van metritis vastgesteld. De verschillende onderzoeken zijn moeilijk te vergelijken, met name vanwege de verschillende proefopzet (selectie dieren/bedrijven, aantal onderzochte dieren/bedrijven, verschillen in diagnostiek). Bij dieren zijn (in tegenstelling tot bij de mens) hart- of longinfecties ten gevolge van Q-fever slechts zelden vastgesteld, met uitzondering van experimentele infecties. Meestal zijn deze longafwijkingen in de geaborteerde foeten niet specifiek.
Morbiditeit/mortaliteit
Tussen 2005 en 2009 zijn abortusuitbraken ten gevolge van C. burnetii aangetoond op geiten- en schapenbedrijven in Nederland. In de meeste gevallen betrof het dieren van melkleverende bedrijven. Uit gegevens uit de monitoring Diergezondheid Kleine Herkauwers van GD in deze periode is gebleken dat op bedrijven met een abortusuitbraak 10-60% van de drachtige dieren aborteerde. Sinds de start van de landelijk verplichte vaccinatie tegen Q-fever (op melkgeiten- en melkschapen bedrijven en op bedrijven met een publieksfunctie) in 2010, zijn geen abortusuitbraken ten gevolge van C. burnetii bij kleine herkauwers meer aangetoond in Nederland. Vaccinatie van kleine herkauwers tegen Q-fever speelt een belangrijke rol in het voorkomen van abortus door C. burnetii en uitscheiding van C. burnetii.
Uitscheiding van de kiem
C. burnetii wordt op verschillende manieren uitgescheiden door een dier. De afgelopen decennia zijn hierover meerdere onderzoeken uitgevoerd. De resultaten hiervan zijn moeilijk te vergelijken, met name omdat de diagnostische methoden in diezelfde periode sterk zijn veranderd. De laatste jaren is bij veel onderzoeken gebruik gemaakt van de PCR-techniek. Excreta waarmee de kiem door herkauwers wordt uitgescheiden:
- Melk: op basis van tankmelkmonitoring hebben melkgeiten- en melkschapenbedrijven vanaf 2009 een Q-fevertatus gekregen. Tankmelkonderzoek is sinds 2010 maandelijks uitgevoerd en in het aflammerseizoen elke twee weken. Individuele uitscheiders van de bacterie zijn op te sporen door individuele melkmonsters te onderzoeken. Vanaf 2018 wordt de tankmelkmonitoring vierwekelijks uitgevoerd, met uitzondering van één bedrijf dat vanwege gewetensbezwaren niet vaccineert tegen Q-fever en enkele bedrijven waar op verzoek van de NVWA intensievere monitoring plaatsvindt. Op het gewetensbezwaarde bedrijf vindt elke twee weken tankmelkonderzoek plaats. Daarnaast zijn door de overheid nog aanvullende eisen gesteld op het gebied van dierbewegingen, hygiëne en een bezoekersverbod.
- Placenta: de bacterie vermeerdert zich sterk in de placenta, met name aan het eind van de dracht en wordt via de nageboorte en het vruchtwater uitgescheiden. De hoeveelheid kiemen die via de placenta wordt uitgescheiden kan erg groot zijn. Waarden van meer dan 109 kiemen per gram placenta zijn bij de ooi vastgesteld. Bij runderen zijn waarden van 107 kiemen per gram placenta aangetoond.
- Foetus
- Vaginale excreta. C. burnetii is een ubiquitair voorkomende kiem. Wanneer de bacterie in vaginale excreta wordt aangetoond is het belangrijk om het aantal kiemen te bepalen. Daarnaast dient dit onderzoek alleen uitgevoerd te worden in de weken direct volgend op een abortus/geboorte. In geval van laag positieve resultaten dient men bedacht te zijn op de mogelijkheid van contaminatie.
- Faeces: in een onderzoek werd bij 40% van zestig met C. burnetii besmette runderen de kiem met een PCR aangetoond in de faeces. Na experimentele besmetting van geiten scheidden alle dieren de kiem uit en deze uitscheiding duurde gemiddeld veertig dagen. Uit onderzoek blijkt dat de rol van mest in de humane Q-koorts uitbraak zeer beperkt is geweest. Op basis van temperatuurmetingen in een mesthoop is geconcludeerd dat de overleving van de kiem in een goed gecomposteerde mesthoop beperkt lijkt te zijn.
- Sperma: in een Pools onderzoek is C. burnetii aangetoond in het sperma van seropositieve stieren. Dit lijkt echter geen belangrijke transmissieroute.
Geconcludeerd mag worden dat de uitscheiding van C. burnetii maximaal is tijdens het geboorteproces, vooral doordat de placenta veel kiemen bevat. In de vaginale excreta van geïnfecteerde dieren zijn kort na de partus ook veel kiemen aanwezig. Het geboorteproces is dus een belangrijke periode voor het verspreiden van de kiem naar koppelgenoten, andere dieren en de mens. Uitscheiding van C. burnetii is beschreven bij zowel serologisch positieve als negatieve dieren. Zodoende is serologisch onderzoek niet geschikt om mogelijke aanstaande uitscheiding rondom de partus te voorspellen. De maximale uitscheidingsduur van de kiem in melk is onbekend, maar kan bij runderen en geiten tenminste enkele maanden bedragen.
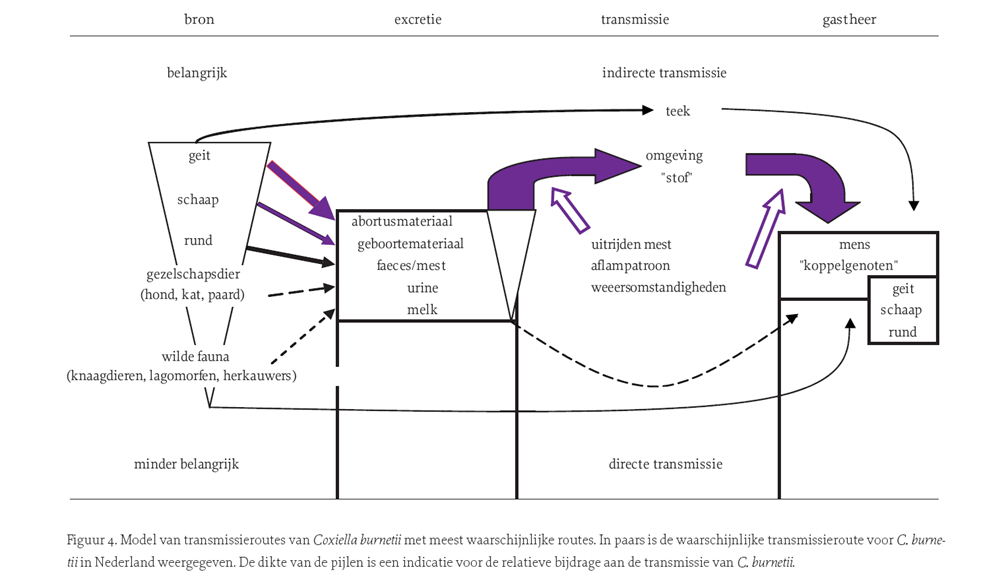
(Roest et al., 2009)
Differentiaaldiagnose
Q-fever is een aangifteplichtige ziekte bij kleine herkauwers. Bevindingen van C. burnetii (immuunhistochemie, PCR of ELISA) bij kleine herkauwers alsook bij runderen moeten worden gerapporteerd aan de NVWA. Aangezien abortus/vroeggeboorte de belangrijkste symptomen van een C. burnetii-infectie zijn, is een afwijkend aantal abortussen (zie www.nvwa.nl) bij kleine herkauwers aangifteplichtig. Abortus kan infectieus of niet-infectieus van aard zijn. Andere infectieuze oorzaken van abortus zijn:
- Chlamydia abortus
- Campylobacter spp.
- Listeria spp.
- Toxoplasma gondii
- Yersinia spp.
- Neospora caninum
- Arcanobacterium pyogenes
- Arcanobacterium pluranimalium
- Border disease virus
- Salmonella spp.
- Staphylococcus spp.
- Streptococcus spp.
- Escherischia coli
- Bacillus licheniformis
- Brucella melitensis
- Schimmels
- Leptospira spp.
- Rift Valley fever virus
- Bunyaviridae
- Alles wat bacteriaemie/viraemie geeft
Diagnose van Q-fever
Pathologie
Standaard wordt bij GD de nageboorte van verworpen en doodgeboren lammeren histologisch onderzocht. Bij Q-fever-verdachte laesies wordt een immunohistochemische kleuring uitgevoerd. Deze kleuring kan de bacterie in het weefsel aantonen (zie foto 1). Bij het rund wordt de nageboorte standaard onderzocht m.b.v. de PCR-techniek. Indien deze niet aanwezig is, wordt dit onderzoek uitgevoerd in de vrucht zelf. Indien de PCR van de placenta bij het rund positief is, wordt de immunohistochemische kleuring uitgevoerd.
NB. Voor abortusdiagnostiek is een volledige inzending van vrucht en nageboorte essentieel om bepaalde diagnoses te kunnen stellen. Zonder placenta zou de diagnose abortus ten gevolge van een infectie met C. burnetii gemist kunnen worden bij kleine herkauwers.
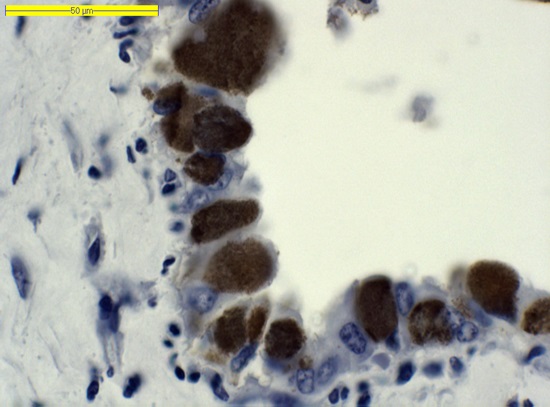
Foto 1. Coxiella burnetii in trophoblastcellen aangetoond met behulp van immuunhistochemische kleuring bij de geit (foto GD)
Isolatie van de kiem
Het aantonen van de bacterie kan door middel van kweek, echter hiervoor is een speciaal toegerust (biosafety level 3) laboratorium nodig. In 2009 is de kiem voor het eerst ook op het Centraal Veterinair Instituut ((CVI), tegenwoordig Wageningen Bioveterinary Research (WBVR)) in Lelystad, geïsoleerd. Diverse moleculair biologische detectiemethoden zijn beschreven en gevalideerd om het genoom van de bacterie aan te tonen. Deze zijn routinematig in gebruik in diverse landen. De meeste PCR-testen zijn gebaseerd op het vermeerderen en detecteren van een conservatief deel van het genoom (Trans PCR). Dit kan met een enkelvoudige PCR of een gevoeliger nested PCR. Omdat C. burnetii celgebonden is, heeft een PCR in serum waarschijnlijk weinig waarde door de afwezigheid van cellen. Ook zijn real time PCR-methodes beschreven die ook kwantitatief gebruikt kunnen worden. In melk kan de PCR gecombineerd worden met immunomagnetische separatiemethoden of silica bindingsmethoden om ook heel kleine aantallen kiemen op te sporen. Een PCR kan DNA van C. burnetii aantonen in paraffine coupes van weefsels, vaginaal slijm (vaginaalswabs) en faeces. Deze PCR-techniek is niet beschikbaar als routine-diagnostiek voor de praktijk.
Er zijn diverse moleculair-biologische typeringsmethodes beschreven. In het algemeen is een nadeel van moleculair biologische detectiemethoden dat er ook afgedode bacteriën aangetoond worden en er wel geconcludeerd kan worden dat er een infectie heeft plaatsgevonden, maar niets geconcludeerd kan worden over de eventuele besmettelijkheid van de aangetoonde kiemen.
In diverse publicaties is de afgelopen jaren beschreven dat er meerdere serotypen van C. burnetii in Nederland zijn gevonden en er is een link beschreven tussen de humane pathogeen en het geitentype.
Serologie
Afweerstoffen tegen C. burnetii zijn aan te tonen met een Complement Bindingsreactie (CBR) zoals deze bijvoorbeeld gebruikt wordt in het internationale handelsverkeer. De CBR-test heeft een matige gevoeligheid en het duurt vrij lang alvorens de CBR afweerstoffen aantoont na infectie. Er zijn diverse ELISA-testen verkrijgbaar, meestal gebaseerd op het aantonen van IgG tegen een combinatie van fase I- en fase II-antigenen. Een vergelijking van testen is slechts in beperkte mate uitgevoerd. Het betreft hier gedateerde studies en de huidige ELISA-testen zijn daarin niet onderzocht. Er zijn geen uitgebreide validatiestudies van de diverse serologische testen beschreven. Voor routine-diagnostiek kan in Nederland gebruik gemaakt worden van de ELISA (GD) en CBR (WBVR) in serummonsters.
Prevalentie van Q-fever
De bacterie wordt wereldwijd (met uitzondering van Nieuw-Zeeland) gevonden. De eerste meldingen van Q-fever zijn afkomstig van Australische en Amerikaanse onderzoekers. Vervolgens is de kiem wereldwijd aangetoond in andere landen bij diverse diersoorten.
Nederland
De Nederlandse situatie is in het verleden bestudeerd, hoewel het destijds wel vaak om lage aantallen dieren ging. In 1954 werd er geen bewijs gevonden voor de aanwezigheid van C. burnetii bij herkauwers. In 1987 werd de situatie bij herkauwers opnieuw onderzocht. In deze studie werd een indirecte ELISA gebruikt. Er werden afweerstoffen tegen C. burnetii aangetoond in 3,5% van 3.603 schapen afkomstig uit 191 koppels. In totaal werden in 52 koppels (27,2%) één of meerdere serologisch positieve schapen gevonden. In een kleine studie onder geiten bleek dat minder dan 1% van de geiten afweerstoffen had. De geteste dieren waren allemaal tussen 0.5 en 1 jaar oud. In 2008 werd in een uitgebreid onderzoek onder ruim 15.000 schapen en geiten de seroprevalentie opnieuw bepaald. In totaal bleek 7,8% van de geiten en 2,4 % van de schapen serologisch positief te zijn. Belangrijke risicofactoren waren melkgeiten en de periode van de late dracht en kort na de dracht. In 2008 is ook een onderzoek uitgevoerd op tankmelkniveau. Hieruit bleek dat 32,9% van de melkgeitenbedrijven PCR-positief was en dat 29,8% van de melkgeitenbedrijven serologisch positief was. Het risico op een positieve tankmelk-ELISA/PCR was het grootst in Zuidoost-Nederland ten opzichte van de rest van Nederland. De gehele Nederlandse uitbraak (zowel humaan als veterinair) is beschreven in een review. In 2016 is op basis van de tankmelkmonitoring vastgesteld dat er geen besmette melkschapen- en melkgeitenbedrijven meer zijn. Sindsdien zijn er geen nieuwe besmettingen meer vastgesteld op deze groep bedrijven. Bij het rund is de diagnose Q-fever bij de groep doodgeboren en verworpen kalveren in 2018 drie maal gesteld, in 2019 vier maal, 2020 drie maal, 2021 eenmaal, 2022 (niet standaard onderzocht), 2023 twee maal (t/m kwartaal 3)
Andere landen
In vele landen zijn prevalenatie-onderzoeken uitgevoerd. Het is niet altijd eenvoudig om studies uit andere landen te vergelijken met elkaar, aangezien er vaak gekozen is voor verschillende studieopzet en gebruik van andere testen. Enkele voorbeelden:
- In het Baskenland werd de seroprevalentie bij schapen op 8.9% geschat en testte minimaal één dier positief in 67.6% van de koppels. Slechts 14.7% van de koppels bevatte meer dan 25% positieve dieren in het koppel. Met het toenemen van de leeftijd bleek de seroprevalentie hoger te liggen.
- In Marmara, Turkije, bleek dat 34 van 42 koppels minimaal één serologisch positief schaap bevatte. In totaal bleek 20% van de schapen serologisch positief te zijn. De seroprevalentie bleek 13%, 28% en 19%, bij respectievelijk lammeren (<10 maanden), primipare ooien (< 1 jaar oud) en ooien die tweemaal hadden afgelammerd.
- Op Cyprus werd de prevalentie bepaald op 48.2% bij geiten en 18.9% bij schapen.
- Op Sardinië werd de seroprevalentie bij schapen bepaald op 9% en 38% van de koppels testte positief. In dezelfde studie bleek de seroprevalentie bij geiten 13% te zijn en 48% van de koppels testte positief.
- In Quebec, Canada, bleken in totaal 137 van de 334 schapen (41%) serologisch positief te zijn en 41 van de 46 koppels (89%) bevatte minimaal één positief schaap.
- In de Verenigde Staten werd een significant hogere seroprevalentie gevonden bij geiten (41.6%) dan bij schapen (16.5%).
- In Newfoundland nam de seroprevalentie onder schapen toe van 3.1% in 1997 naar 23.5% in 2000, waarbij 15.6% van de geiten antilichamen had.
- De seroprevalentie onder schapen in Turkije was 10.5% en 62% in Sudan.
In de afgelopen jaren zijn veel artikelen over Q-feverprevalenties en risicofactoren bij geiten, schapen en runderen gepubliceerd. Geconcludeerd mag worden dat de resultaten van de onderzoeken in de genoemde landen verschillend zijn, zowel op dier- als op koppelniveau. Het is echter nauwelijks mogelijk om de diverse onderzoeken goed met elkaar te vergelijken, omdat de wijze van selectie van bedrijven (en dieren) en/of de diagnostische testen verschillend waren. Daarnaast zijn weinig tot geen gegevens beschikbaar over de eigenschappen (sensitiviteit en specificiteit) van de gebruikte testen. De Nederlandse situatie aangaande de seroprevalentie in 2008 is in 2012 gepubliceerd. Ook de prevalentie onder Nederlandse dierenartsen werkzaam in de landbouwhuisdierensector is in 2012 beschreven. De prevalentie was hoog, ruim 65%, en de belangrijkste risicofactor voor dierenartsen bleek de mate van contact met landbouwhuisdieren te zijn. Ook uit onderzoek in andere landen blijkt dat mensen met veel diercontacten (zogenoemde “people at risk”) meer risico lopen op een infectie met Q-fever. In Australië wordt een humaan vaccin ingezet om deze groep mensen te beschermen tegen infectie met C. burnetii.
Aanpak besmette bedrijven
Bij de aanpak van besmette bedrijven kan onderscheid gemaakt worden tussen een aantal methoden, namelijk (a) vaccinatie, (b) het gebruik van antibiotica, en (c) overige maatregelen.
Vaccinatie
Vaccins tegen C. burnetii kunnen in twee groepen worden verdeeld, namelijk vaccins die gebaseerd zijn op de fase I en vaccins die gebaseerd zijn op de fase II van de bacterie. Beide groepen vaccins kunnen gemaakt zijn van hele bacteriën of bacteriefracties. De resultaten van de vaccins zijn niet altijd hetzelfde. Daarbij zijn er soms ernstige reacties op de injectieplaats waargenomen.
Na vaccinatie met een fase I-vaccin bij het rund is nagegaan of dit invloed had op de mate van uitscheiding van C. burnetii in de melk. Bij de niet-gevaccineerde dieren bleek 24% uitscheider te zijn na besmetting, bij de gevaccineerde runderen was dit 1%. Een vermindering van de uitscheiding is ook aangetoond in een ander onderzoek, waarbij tevens een bescherming tegen het optreden van abortus werd aangegeven. Bij runderen zijn fase I- en fase II-vaccins nog niet met elkaar vergeleken. Verwacht mag worden dat, net als bij geiten, fase I-vaccins het meest effectief zijn. Er is geen informatie over het effect van vaccinatie op transmissie van de bacterie. Dieren worden seropositief na vaccinatie. Er zijn geen markervaccins of markertesten beschikbaar. In Nederland zijn kleine herkauwers gevaccineerd in verband met het grote aantal humane gevallen. Dit vaccin is ook geregistreerd om runderen te vaccineren.
Uit meerdere studies is gebleken dat vaccinatie van schapen en geiten vóór hun eerste dracht leidt tot een aanzienlijke reductie van het aantal abortussen alsook tot verminderde uitscheiding van C. burnetii. Uit Belgisch onderzoek, dat werd gepubliceerd in 2021, bleek koppels geiten waar de vaccinatie intermitterend, niet-volledig en niet-gesynchroniseerd was uitgevoerd, significant vaker en langer C. burnetii uitscheidden dan koppels waar de vaccinatie doorlopend, volledig en gesynchroniseerd was uitgevoerd.
Sinds 2010 geldt in Nederland een vaccinatieplicht voor Q-fever voor melkleverende bedrijven met meer dan 50 schapen en/of geiten en voor bedrijven met een publieksfunctie en kleine herkauwers die naar shows toegaan. Soms wordt er door melkschapen- en melkgeitenhouders melding gedaan van bijwerkingen ten gevolge van de vaccinatie tegen Q-koorts. Deze bijwerkingen zijn in lijn met de bijwerkingen zoals die in de bijsluiter worden genoemd. De ervaring die wordt gedeeld is dat bijwerkingen van de vaccinatie tegen Q-fever kunnen worden beperkt wanneer de vaccinatie wordt uitgevoerd in een periode dat de dagen lengen, de weersomstandigheden gematigd en stabiel zijn en wanneer stress wordt vermeden. Let op! Er gelden wettelijke regels omtrent de vaccinatie tegen Q-fever. (www.rijksoverheid.nl/onderwerpen/diergezondheid/vraag-en-antwoord/kleine-herkauwers). In 2023 is het Q-fever vaccin geregistreerd voor schapen.
Antibiotica
C. burnetii is in vitro gevoelig voor meerdere antibiotica, onder andere tetracyclines en macroliden. Het is in de praktijk erg moeilijk om de effectiviteit in vivo te meten, met name omdat het erg moeilijk is om de kiemen te kweken en te tellen. Mogelijk kan hier een kwantitatieve PCR-methode ingezet worden, echter daarmee worden ook afgedode kiemen gedetecteerd.
Bij de behandeling met antibiotica wordt het injecteren van langwerkende oxytetracyclines als de beste aanpak beschouwd, hoewel betwijfeld moet worden of daarmee de uitscheiding via placenta, vaginale uitvloeiing en melk tegengegaan wordt. Bij kleine herkauwers lijkt behandeling met antibiotica op besmette bedrijven niet effectief.
Overige maatregelen
Opsporen en afvoeren besmette dieren
Het opsporen en afvoeren van besmette dieren die kiemen uitscheiden via de excreta (o.a. mest, placenta en vaginale uitvloeiing) is een van de maatregelen om overdracht van kiemen zowel binnen als tussen bedrijven te reduceren of te voorkomen. Directe of aërogene overdracht tijdens de geboorte of abortus spelen een belangrijke rol bij de besmetting van koppelgenoten of dieren uit andere koppels. Deze besmetting kan ook op een later tijdstip plaatsvinden omdat de kiem waarschijnlijk lang persisteert in de omgeving. Het opsporen van uitscheidende dieren is moeilijk, onder andere omdat uitscheiding intermitterend is, dieren seropositief blijven terwijl ze de kiem niet meer uitscheiden en niet alle dieren seroconverteren. Echter, het opsporen van individuele uitscheiders op tankmelk C. burnetii PCR positieve bedrijven is beschreven als mogelijkheid om bedrijven tankmelk PCR negatief te krijgen. In Frankrijk is bij zestig runderen die PCR-positief waren in faeces en/of melk en/of vaginale uitvloeiing, nagegaan in welke mate ze positief waren in de drie genoemde excreta. Van de zestig runderen bleek slechts zeven procent positief te zijn in alle drie de excreta, vijftien procent was positief in twee van de drie excreta en 78% was PCR-positief in een van de drie excreta.
Het opsporen en afvoeren van uitscheidende runderen heeft een gunstig effect op de infectiedruk van de omgeving, lijkt effectief op bedrijfsniveau en is dus aan te raden.
Algemene maatregelen
Naast de bovengenoemde maatregelen is een aantal algemene maatregelen wenselijk, zoals:
- Algemene hygiëne.
- Het vernietigen van strooisel dat mogelijk besmet is met baarmoederinhoud (amnionvloeistof, nageboorte, etc.) die vrij is gekomen tijdens en na de geboorte.
- Het vernietigen van placenta’s en verworpen vruchten. Hiermee moet hygiënisch worden omgegaan en de placenta’s en verworpen vruchten moeten zo snel mogelijk worden opgehaald door de kadaverophaaldienst.
- Reinigen en desinfecteren van vloeren, voertuigen en gebruiksvoorwerpen. Daarbij moet wel in ogenschouw worden genomen dat de kiem bestand is tegen veel desinfectantia (zie Hoofdstuk Desinfectie).
- Geen dieren aankopen en zorgen voor een goede scheiding met dieren van naburige bedrijven.
Maatregelen in kader volksgezondheid
Landbouwhuisdieren worden in het algemeen beschouwd als de belangrijkste bron van humane Q-fever-infecties, alhoewel ook andere diersoorten als reservoir van C. burnetii kunnen dienen. Gezien het risico voor de mens is het zinvol om meer onderzoek te doen bij humane gevallen van Q-fever met als doel de bron op te sporen en verdere verspreiding vanuit die bron te voorkomen. Indien infecties worden vastgesteld waarbij uitscheiding van kiemen optreedt of zeer waarschijnlijk is, is het gewenst om maatregelen te nemen om humane infecties zoveel mogelijk te voorkomen. Belangrijk is met name een optimale hygiëne rond het afkalven en aflammeren. Zwangere vrouwen moeten deze “activiteiten” vermijden. Omdat de kiem ook in melk wordt uitgescheiden, zou alle melk gepasteuriseerd moeten worden. Hierbij kan gerefereerd worden aan de eisen die in Frankrijk aan besmette bedrijven gesteld worden. Van het onderzoek dat is gedaan naar de effectiviteit van pasteurisatie zijn echter slechts summiere beschrijvingen te vinden.
In meerdere landen wordt Q-fever als een beroepsziekte gezien (voor veehouders, slachthuispersoneel, dierenartsen, mensen met andere agrarische beroepen, plattelandspopulaties). In Australië bijvoorbeeld wordt in een centraal register voor alle risicogroepen bijgehouden of mensen seropositief en al dan niet gevaccineerd zijn.
Preventie van Q-fever
Ter preventie moet gedacht worden aan het voorkomen van infecties bij mens en dier. Kleine herkauwers zijn op basis van literatuur een belangrijke bron van Q-koorts bij mensen. Vaccinatie van kleine herkauwers is zeer effectief gebleken in de preventie van abortus en vermindering van uitscheiding. Echter, door vaccinatie zullen nooit alle infecties bij mensen kunnen worden voorkomen, aangezien ook vele andere diersoorten de bacterie kunnen uitscheiden.
Besmetting met C. burnetii kan waarschijnlijk aërogeen (aërosolen van ingedroogde faeces en vruchtwater), door opname van geïnfecteerde nageboorte, vaginale uitvloeiing, contact met besmette wol of huiden, of door consumptie van besmette rauwe melk of kaas.
De kiemen kunnen waarschijnlijk met de wind over grotere afstanden overgebracht worden. In een Frans onderzoek werden humane gevallen geassocieerd met een mistralwind die een maand eerder had plaatsgevonden in een periode kort na aanvang van het lammerseizoen. Mogelijk kan de infectie tussen dieren ook over grotere afstand via de wind worden overgebracht. Het is belangrijk te voorkomen dat dieren grote hoeveelheden kiemen uitscheiden, die vervolgens via direct contact of aërogeen overgebracht kunnen worden naar andere dieren of mensen. Risico’s op infecties op bijvoorbeeld zorgboerderijen zouden moeten worden onderzocht en beperkt.
Naast de al eerder genoemde preventieve maatregelen, is het zinvol om aandacht te besteden aan de mogelijke besmetting via sperma, insecten en ratten:
- Mogelijk kan de infectie overgebracht worden via sperma.
- In een Egyptisch onderzoek zijn vlooien onderzocht op meerdere bacteriën waaronder C. burnetii. In twee vlooien is de bacterie aangetroffen. Ook kan de infectie via teken worden overgebracht. In hoeverre de infectie in Nederland ook via insecten wordt overgebracht, is onbekend.
- Van boerderijen afkomstige bruine, wilde ratten zijn serologisch onderzocht op C. burnetii. Met name op bedrijven met melkvee en schapen werd de hoogste seroprevalentie (tot 53%) vastgesteld. Op grond van deze resultaten werd gesuggereerd dat wilde ratten mogelijk een reservoir in het Verenigd Koninkrijk vormen voor besmetting met Q-fever. Datzelfde geldt voor katten, als predatoren van deze ratten.
Regelgeving
In Nederland bestaat aangifteplicht voor Q-fever bij kleine herkauwers. Aangezien abortus het belangrijkste symptoom is van Q-fever bij kleine herkauwers, geldt voor een afwijkend aantal abortussen bij kleine herkauwers een meldplicht (zie www.nvwa.nl). De ziekte is ook aangifteplichtig bij de mens. Bij het rund is er geen aangifteplicht bij klinische verdenkingen, echter laboratoriumbevindingen van C. burnetii (immuunhistochemie, PCR of ELISA) bij runderen moeten, evenals bij kleine herkauwers, worden gerapporteerd aan de NVWA.
Actualiteiten en maatregelen staan tevens vermeld in de factsheet Q-fever van het ministerie van LNV.
Websites
- Wageningen University and research
- Department for Environment Food & Rural Affairs
- World Organisation for Animal Health (OIE)
- Royal GD
- RIVM
- NVWA